OneKensaの概要
OneKensaは、一般的に健康な人々のがんリスクを特定するのに役立つアルゴリズムを備えた腫瘍バイオマーカーテストのパネルを使用した新しいがんリスクテストです。性別に応じて、血液検体は、FDAが承認した6つまたは7つの腫瘍バイオマーカーについて分析されます。早い開発の段階。個人のがんリスクを計算するために、OneKensaは、これらの血液検査の結果を年齢や性別などの個人情報とともに組み込む機械学習アルゴリズムを採用しています。これにより、腫瘍バイオマーカーを個別に検査する場合と比較して、検査の精度をさらに向上させることができます。
腫瘍マーカーのテストは、20 / 20GeneSystemsのCLIAラボで ロシュCobase411プラットフォーム。FDA承認のロシュのIVD試薬キットは、メーカーの仕様に従って使用されます。個々の腫瘍マーカーテストの結果は、機械学習独自のアルゴリズムを使用してリスクスコアを計算し、患者レポートを生成するために使用されます。OneKensaレポートは、患者に次の情報を提供します。1)個々の5(男性)または6(女性)バイオマーカーレベル、機械学習アルゴリズムを使用して計算された全体的ながんリスクスコア、およびリスクの高い人の臓器系(原発腫瘍が発生している可能性が高い胃腸、泌尿生殖器など)。
スクリーニングのための腫瘍マーカー
血液中の腫瘍マーカーは、患者がまだ無症候性である間に、初期段階で癌を検出する可能性があります。定期的に医師の診察を受ける患者(例:年1回の健康診断)の場合、通常、年1回の診察時またはその前に採血し、一般的な健康状態のマーカー(コレステロール、肝酵素など)のパネルを分析します。腫瘍マーカーは簡単に追加できます(一部の国ではすでに追加されています)。何年にもわたって、さまざまな種類の癌について多くの腫瘍マーカーが特定されてきました。しかし、臨床使用のためにUS-FDAによって開発され、承認されたタンパク質腫瘍マーカーイムノアッセイはほんの一握りです[1]。残念ながら、これまでのところ、単一の腫瘍マーカー(PSAとその有用性が現在疑問視されていることを除く)は、癌の一般的な早期発見における日常的な使用を保証するために著しく高いレベルの特異性または感度を示していません。個々のバイオマーカーの限界に対処するために、多くの学術および業界の科学的研究により、確立されたバイオマーカーを最適化されたマルチバイオマーカーパネルに組み合わせることで診断精度が向上し、そのようなパネルが改善された癌検出ツールになることが実証されています[2-6]。
マーカーのパネルに基づくテストは、マーカーの発現の差異、異なる患者によるマーカーレベルの固有の変動、および/または複数のマーカーの低レベルの変化を組み合わせることによって達成される感度と特異性のレベルの増加につながる癌サブタイプの病因の違いにより、パフォーマンスが向上します初期の段階で癌の存在を示すため。卵巣がんの検出用のOVA1 [7、8]や前立腺がんのスクリーニング用のphi [9、10]など、いくつかのパネルが臨床的に承認されており、感度と特異性のレベルが向上しています。

OneKensa腫瘍マーカーパネル
OneKensaは、5つまたは6つの腫瘍マーカーのパネルです。
男性パネル: AFP, CEA, CA19-9, CYFRA21-1, PSA
女性パネル: AFP, CEA, CA19-9, CYFRA21-1, CA125, CA15-3
CEA: 癌胎児性抗原(CEA)は、主に結腸や消化管の他の臓器の疾患に関連するタンパク質です。マーカーは、乳がんと肺がんにも関連しています。結腸直腸癌患者の管理(モニタリング)での使用が承認されています。
CA 15-3: CA 15-3(Cancer Antigen 15-3)は乳がんマーカーです。 高率は、結腸、胃、腎臓、肺、卵巣、子宮、膵臓、肝臓などの他の癌にも当てはまります。
CA 19-9: CA 19-9(Cancer Antigen 19-9)は、主に結腸直腸癌、膵臓癌、胃癌、胆管癌に関連するタンパク質です。膵臓がん患者のモニタリングでの使用が承認されています。
CA 125: 血清CA 125(Cancer Antigen 125)タンパク質値は、浸潤性上皮性卵巣癌患者の疾患経過を監視するのに役立ちます。持続的に上昇するCA125値は、悪性疾患に関連している可能性があります。35 U / mL以上のCA125値は、残存腫瘍の存在を示していることがわかりました。CA 125のレベルの上昇は、子宮内膜および卵管の癌にも見られます。また、肺がんの一部の患者の血清でも上昇しています。
AFP: AFP(アルファ-1-フェトプロテイン(AFP)は肝臓関連タンパク質であり、ウイルス性肝炎、肝臓の肝硬変、肝臓癌、精巣癌、卵巣癌などの肝臓疾患で一般的に上昇します。癌のモニタリングによく使用されます。進行。
CYFRA 21-1: サイトケラチン-19(CYFRA 21-1)の断片は、肺がん、頭頸部がん、乳がんに関連していますが、多くの良性状態でも上昇しています。CYFRA 21-1は、肺がんの進行のモニタリングでの使用が承認されています。CYFRA 21-1は、子宮がん、食道がん、膀胱がんにも使用できます。
癌検出のための腫瘍マーカー
血液中の腫瘍タンパク質は、患者がまだ無症候性である間に、初期段階で癌を検出する可能性があります。定期的に医師の診察を受ける患者(例:年1回の健康診断)の場合、通常、年1回の診察時またはその前に採血し、一般的な健康状態のマーカー(コレステロール、肝酵素など)のパネルを分析します。腫瘍マーカーは簡単に追加できます(一部の国ではすでに追加されています)。何年にもわたって、さまざまな種類の癌について多くの腫瘍マーカーが特定されてきました。しかし、臨床使用のためにUS-FDAによって開発され、承認されたタンパク質腫瘍マーカーイムノアッセイはほんの一握りです[1]。不幸にも、今日まで、単一の腫瘍マーカー(PSAとその有用性が現在疑問視されていることを除く)は、癌の一般的な早期発見における日常的な使用を保証するために著しく高いレベルの特異性または感度を示していません。個々のバイオマーカーの限界に対処するために、多くの学術および業界の科学的研究により、確立されたバイオマーカーを最適化されたマルチバイオマーカーパネルに組み合わせることで診断精度が向上し、そのようなパネルが改善された癌検出ツールになることが実証されています[2-6]。
マーカーのパネルに基づくテストは、マーカーの発現の差異、異なる患者によるマーカーレベルの固有の変動、および/または複数のマーカーの低レベルの変化を組み合わせることによって達成される感度と特異性のレベルの増加につながる癌サブタイプの病因の違いにより、パフォーマンスが向上します。より早い段階での癌の存在を示します。卵巣がんの検出用のOVA1 [7、8]や前立腺がんのスクリーニング用のphi [9、10]など、いくつかのパネルが臨床的に承認されており、感度と特異性のレベルが向上しています。
- Ludwig JA,Weinstein JN 癌の病期分類、予後および治療法の選択におけるバイオマーカーNat Rev Cancer。 2005年11月; 5(11):845-56。
- Cohen JD、Li L、Wang Y、他 多検体血液検査による外科的に切除可能な癌の検出と位置特定。科学2018; 359:926。
- Nolen B、Brand R、Prosser D、Velikokhatnaya L、Allen P、他 大規模な前向きコホート研究における膵臓癌の早期発見ツールとしての診断前血清バイオマーカー。PLoS ONE 2014、9(4)。e94928。
- Molina R、Marrades R、Auge J、他 肺がんの6つの血清腫瘍マーカーの組み合わせパネルの評価。Am J Respir Crit Care Med(2015)10月。土井:10.1164 /rccm.201404-0603oc。
- アンダーソンGL、マッキントッシュM、ウーL、他。選択された卵巣癌バイオマーカーのリードタイムの評価:ネストされたケースコントロール研究。国立癌研究所のJNCIジャーナル。2010; 102(1):26-38。doi:10.1093 / jnci / djp438。
- Cohen JD et al。、「膵臓癌の早期発見のための循環腫瘍DNAとタンパク質バイオマーカーベースのリキッドバイオプシーの組み合わせ、PNAS(2017)。pnas.org/cgi/doi/10.1073/pnas.1704961114
- Moore RG、Miller MC、DisilvestroPなど。骨盤腫瘤のある女性における卵巣悪性腫瘍アルゴリズムのリスクの診断精度の評価。ObstetGynecol。2011; 118:280–28
- Montagnana M,Benati M, Danese E。上皮性卵巣癌診断における循環バイオマーカー:現在から将来の展望まで。Ann Transl Med. 2017年7月; 5(13):276。土井:10.21037 /atm.2017.05.13。
- Filella X、GiménezN。前立腺癌の検出のための[-2] proPSAおよびProstateHealth Index(phi)の評価:系統的レビューとメタ分析。Clin Chem Lab Med 2013; 51:729。
- ローブS、カタロナWJ。 前立腺健康指数:前立腺癌を検出するための新しいテスト Ther AdvUrol.20144月; 6(2):74–77。土井:10.1177 / 1756287213513488
シリアルテストの重要性
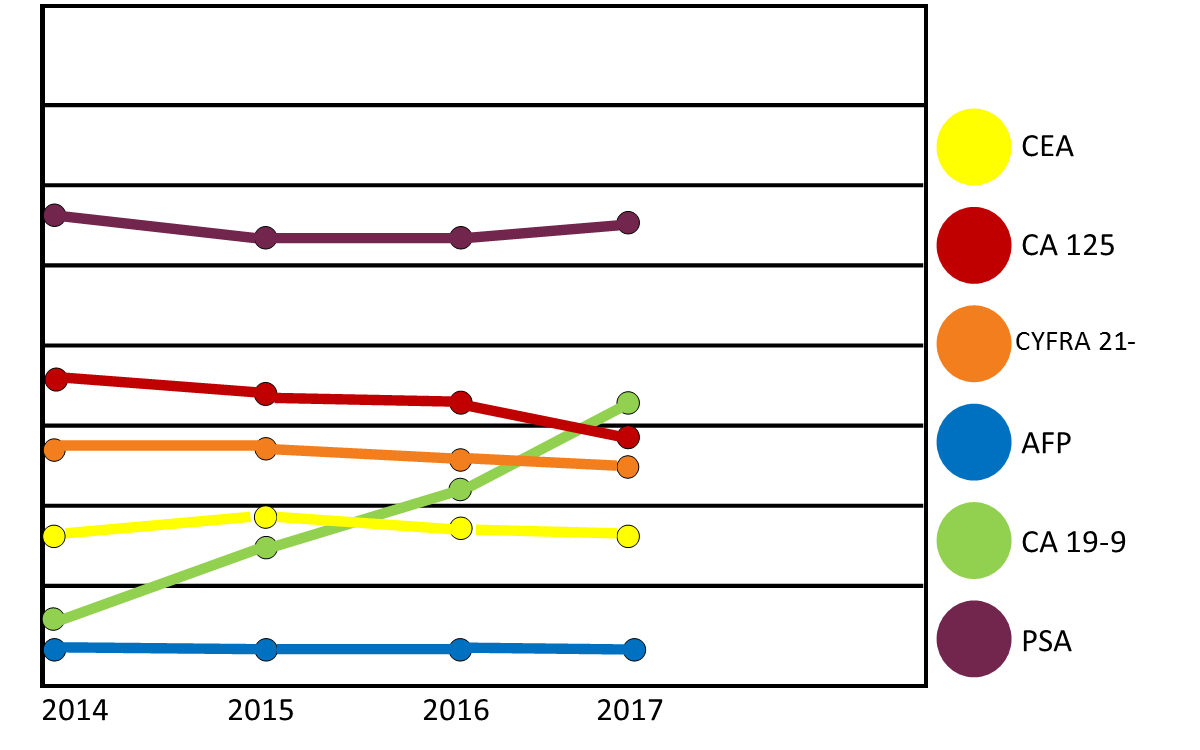
現在、20/20のOneKensaアルゴリズムは、単一の血清サンプルの測定から派生しています。しかし、現在、CA-125とCEA、および他のいくつかの腫瘍タンパク質のレベルが、その後卵巣癌、膵臓癌、および前立腺を有することが判明した患者からの診断前の連続的に採取されたサンプルで急激に上昇するという証拠があります[11 -15]。たとえば、卵巣癌に関する2つの前向き試験から得られたROCAアルゴリズムは、CA-125の感度を標準カットオフに基づく58.0%から縦方向に得られたアルゴリズムを使用した89.4%に増加させました[11]。
スクリーニングアルゴリズムのさらなる開発は、特定のバイオマーカーの静的または単にしきい値レベルではなく、マーカー速度、経時的なマーカーレベルの変化を比較することです。がん患者からの縦断的データを使用してアルゴリズムを変更する機能は、テストのパフォーマンスを大幅に向上させる可能性があります。
- Menon U、Ryan A、Kalsi J、他 連続バイオマーカー測定を使用するリスクアルゴリズムは、英国の卵巣がんスクリーニング共同試験の単一閾値ルールと比較して、スクリーニングで検出されたがんの数を2倍にします。J Clin Oncol 2015; 33:2062–71。
- スケートS、メノンU、マクドナルドN、ローゼンタールA、オラムD、ナップR、ジェイコブスI.閉経後の女性の前臨床検出のためのシリアルCA-125値からの卵巣がんリスクの計算。J ClinOncol。2003; 21:206s-210s。
- Menon U、Gentry-Maharaj A、Hallett R、et al:卵巣癌のマルチモーダルおよび超音波スクリーニングの感度と特異性、および検出された癌の病期分布:卵巣癌スクリーニングの英国共同試験(UKCTOCS)の有病率スクリーニングの結果。ランセットオンコル; 10:327-40、2009。
- Nolen B、Brand R、Prosser D、Velikokhatnaya L、Allen P、他 大規模な前向きコホート研究における膵臓癌の早期発見ツールとしての診断前血清バイオマーカー。PLoS ONE 2014、9(4)。e94928。
- ツマRS。PSA速度の重要性の測定。JNCI:Journal of the National Cancer Institute、第103巻、第6号、2011年3月16日、454〜461ページ
「機械学習」アルゴリズム
機械学習は人工知能(AI)の一種であり、コンピューターシステムは新しいデータを継続的に処理して組み込み、時間の経過とともにその出力を微調整することができます。患者のバイオマーカーレベルを関連する臨床因子データと組み合わせて解釈するために使用されるアルゴリズムは機械学習から派生しているため、このアルゴリズムは定期的なレビューと再定義に適しています。現在のアルゴリズムはこれまでに実施された厳密な研究に基づいて修正されていますが、20/20 GeneSystems、Inc。は、既存の患者データセットの拡大に合わせてアルゴリズムの定期的なレビューを実施することをお約束します。OneKensa後の患者フォローアップからの結果データを20 / 20GeneSystems、Inc。に提供することにより、